Dung dịch NaOH và dung dịch CH3COONa có cùng nồng độ mol/l. Giá trị pH của hai dung dịch tương ứng là x và y. Quan hệ giữa x và y là (giả sử cứ 100 ion CH3COO- thì có 1 ion thủy phân).
A. y = 100x
B. y = 2x
C. y = x+2
D. y = x-2
Dung dịch HCl và dung dịch CH3COOH có cùng nồng độ mol/lít. Giá trị pH tương ứng của dịch tương ứng là x và y. Quan hệ giữa x và y là ( giả thiết cứ 100 phân tử 2 dung CH3COOH thì có 1 phân tử điện li)
A. y = 100x
B. y = 2x
C. y = x-2
D. y = x+2
Đáp án D
HCl → H++ Cl-
[H+] = a M ; suy pH = -log a = x
![]()
Cứ 100 phân tử CH3COOH thì có 1 phân tử điện li nên [H+] = a/100 M suy ra pH = -log (a/100) = y
Do đó y-x = 2
Dung dịch HCl và CH3COOH có cùng nồng độ. pH của hai dung dịch này tương ứng là x và y. Cứ 100 phân tử CH3COOH thì có 1 phân tử phân li. Quan hệ giữa x và y là:
A. y = 100x
B. y = 2x
C. y = x – 2
D. y = x + 2
Đáp án D
Cứ 100 phân tử CH3COOH thì có 1 phân tử phân li
⇒ nH+/HCl = 100nH+/ CH3COOH
Mà dung dịch HCl và CH3COOH có cùng nồng độ
⇒ [H+/HCl] = 100[H+/ CH3COOH]
⇒ -log[H+/HCl] = -2 - log[H+/ CH3COOH]
⇒ x = -2 + y ⇒ y = x + 2
Đáp án D.
Cho 2 dung dịch HCl và CH3COOH có cùng nồng độ. Dung dịch HCl có pH = x, dung dịch CH3COOH có pH = y. Bỏ qua sự điện li của nước, các dung dịch ở cùng nhiệt độ phòng. Biết ở nhiệt độ phòng, cứ 100 phân tử CH3COOH thì có 1 phân tử phân li ra ion. Mối liên hệ của x và y là:
A. x = y - 2
B. y = x – 2
C. x = 2y
D. y = 2x
Không mất tính tổng quát, ta đặt:
![]()
Vì HCl là chất điện li mạnh nên ta có phương trình điện li như sau:
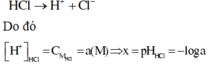
Vì CH3COOH là chất điện li yếu nên ta có phương trình điện li như sau
Xét cân bằng điện li: CH3COOH ⇌ CH3COO- + H+
Nồng độ ban đầu: aM 0
Nồng độ phân li: 0,01a M → 0,01a M
Nồng độ cân bằng: 0,99a M 0,01a M
Ta có
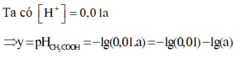
![]()
Đáp án A.
Nhỏ từ từ dung dịch NaOH 1M vào dung dịch chứa X mol NaHCO3 và y mol Ba(HCO3) 2. Đồ thị biểu diễn sự phụ thuộc giữa số mol ion CO32- tự do trong dung dịch vào thể tích dung dịch NaOH như sau:

Giá trị của x và y tương ứng là
A. 0,3 và 0,1
B. 0,2 và 0,2
C. 0,3 và 0,3.
D. 0,1 và 0,2
Đáp án D
Khi thêm NaOH vào dung dịch thì xảy ra phản ứng
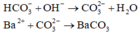
Tại thời điểm 0,2 mol NaOH mới có ion CO32- tự do trong dung dịch
số mol của Ba2+ là 0,2 mol y = 0,2
Tại thời điểm 0,5 mol NaOH thì lượng CO32- tự do trong dung dịch là tối đa
x+ 2y = 0,5 ( bảo toàn nguyên tố C) x= 0,1
Nhỏ từ từ dung dịch NaOH 1M vào dung dịch chứa X mol NaHCO3 và y mol Ba(HCO3) 2. Đồ thị biểu diễn sự phụ thuộc giữa số mol ion CO32- tự do trong dung dịch vào thể tích dung dịch NaOH như sau:
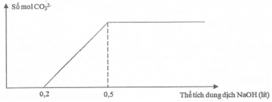
Giá trị của x và y tương ứng là
A. 0,3 và 0,1
B. 0,2 và 0,2
C. 0,3 và 0,3
D. 0,1 và 0,2
Trộn 2 dung dịch: B a H C O 3 2 , N a H S O 4 có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
A. N a + , H C O 3 - v à S O 4 2 - .
B. B a 2 + , H C O 3 - v à N a + .
C. N a + , H C O 3 - .
D. N a + v à S O 4 2 - .
Trộn hai dung dịch Ba HCO 3 2 và NaHSO 4 có cùng nồng độ mol với nhau theo tỉ lệ thể tích 1 : 1 thu được kết tủa và dung dịch. Bỏ qua sự thủy phân của các ion và sự điện li của nước, các ion có mặt trong dung dịch Y là
A. Na + , SO 4 2 -
B. Ba 2 + , HCO 3 2 - , Na +
C. HCO 3 2 - , Na +
D. SO 4 2 - , HCO 3 2 - , Na +
Đáp án C
Ba(HCO3)2 + NaHSO4® BaSO4 ↓+ NaHCO3 + CO2 ↑+ H2O
Vậy sau phản ứng, trong dung dịch còn lại các ion Na+ và HCO3-.
Trộn 2 dung dịch: Ba(HCO3)2; NaHSO4 có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1:1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
![]()
![]()
![]()
![]()
Trộn 2 dung dịch: Ba(HCO3)2 ; NaHSO4 có cùng nồng độ mol/l với nhau theo tỷ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. ( Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
A. Na+, HCO3- và SO42-
B. Ba2+, HCO3- và Na+
C. Na+ và SO42-
D. Na+, HCO3-